-

Мы находимся
Не стесняйтесь обращаться к нам, если у Вас возникнут вопросы!
Email: apteka-euromed@mail.ru
Тел: +7 (812) 907-10-23

Описание
Регистрационный номер: ЛП-003405
Торговое наименование препарата: Стиварга®/Stivarga®
Международное непатентованное наименование: Регорафениб/ Regorafenib
Лекарственная форма: таблетки, покрытые пленочной оболочкой
Состав:
Одна таблетка, покрытая пленочной оболочкой, содержит:
Действующее вещество: регорафениб - 40,00 мг.
Вспомогательные вещества: целлюлоза микрокристаллическая - 100,00 мг, кроскармеллоза натрия - 154,00 мг, магния стеарат - 3,60 мг, повидон-25 - 160,00 мг, кремния диоксид коллоидный - 2,40 мг.
Пленочная оболочка: опадрай II™ 85G35294 розовый (железа оксид красный Е172 - 0,0648 мг, железа оксид желтый Е172 - 0,0732 мг, лецитин - 0,42 мг, макрогол/PEG 3350 - 1,482 мг, поливиниловый спирт, частично гидролизованный - 5,28 мг, тальк - 2,40 мг, титана диоксид Е171- 2,28 мг) - 12,00 мг.
Описание
Овальные таблетки, покрытые пленочной оболочкой, светло-розового цвета, на одной стороне методом выдавливания нанесено «40», на другой стороне - «BAYER».
Фармакотерапевтическая группа
Противоопухолевый препарат, ингибитор протеинкиназы.
Код АТХ: L01XE21
Фармакологические свойства
Фармакодинамика
Механизм действия
Регорафениб является ингибитором многочисленных протеинкиназ, включая киназы, участвующие в ангиогенезе опухоли (VEGFR1,-2,-3, TIE2), онкогенезе (KIT, RET, RAF-1, BRAF, BRAFv600E), а также входящие в состав микроокружения опухоли (PDGFR, FGFR). В частности, регорафениб ингибирует мутантную киназу KIT, ключевой онкогенный фактор в развитии стромальных опухолей желудочно-кишечного тракта. Благодаря этому регорафениб блокирует пролиферацию опухолевых клеток. В доклинических исследованиях было показано, что регорафениб оказывает выраженное противоопухолевое действие на широком спектре опухолевых моделей, включая колоректальный рак и гастроинтестинальные стромальные опухоли. Эффект препарата связан с его антиангиогенным и антипролиферативным воздействием. Кроме того, регорафениб показывает антиметастатическое действие in vivo. Основные метаболиты препарата в организме человека (М-2 и М-5) по своей эффективности на моделях in vitro и in vivo сопоставимы с регорафенибом.
Фармакокинетика
Всасывание
После приема таблеток регорафениба его средняя относительная биодоступность по сравнению с раствором для приема внутрь составляет 69-83 %.
Среднее значение пикового уровня регорафениба в плазме крови (Cmax) составляет около 2,5 мг/л приблизительно через 3-4 часа после однократной пероральной дозы регорафениба 160 мг (4 таблетки по 40 мг).
Наибольшая концентрация регорафениба и его основных фармакологически активных метаболитов М-2 (N-оксид) и М-5 (N-оксид и N-дезметил) достигается после приема завтрака с низким содержанием жиров по сравнению с приемом после завтрака с высоким содержанием жиров или приемом натощак. По сравнению с приемом натощак экспозиция регорафениба увеличивается на 48 % при приеме после завтрака с высоким содержанием жиров и на 36 % при приеме после завтрака с низким содержанием жиров. По сравнению с приемом натощак, экспозиция метаболитов М-2 и М-5 выше при приеме регорафениба после завтрака с низким содержанием жиров и ниже при приеме после завтрака с высоким содержанием жира.
Распределение
Кривая зависимости «концентрация-время» демонстрирует несколько пиков как для регорафениба, так и для его основных циркулирующих метаболитов, в течение 24 часов после приема дозы, что связано с печеночно-кишечной рециркуляцией препарата. Связь регорафениба с белками плазмы крови in vitro высокая и составляет 99,5 %.
Метаболизм
Метаболизм регорафениба осуществляется, главным образом, в печени путем окисления, опосредованного изоферментом CYP3A4, а также путем глюкуронирования, опосредованного UGT1A9. В плазме выявляются два основных и шесть второстепенных метаболитов регорафениба. Основные циркулирующие в плазме крови метаболиты регорафениба М-2 (N-оксид) и M-5 (N-оксид и N-дезметил) обладают фармакологической активностью и в равновесном состоянии имеют концентрации, сходные с концентрацией регорафениба.
In vitro связь М-2 и М-5 с белками крови выше, чем у регорафениба и составляет 99,8 % и 99,95 % соответственно.
Метаболиты могут быть восстановлены и гидролизированы микрофлорой желудочнокишечного тракта, при этом возможно повторное всасывание неконъюгированного препарата и его метаболитов (печеночно-кишечная рециркуляция).
Выведение
Период полувыведения регорафениба и его метаболита М-2 из плазмы составляет от 20 до 30 часов после приема внутрь. Средний период полувыведения метаболита М-5 составляет около 60 часов (40 - 100 часов).
Приблизительно 90 % дозы препарата, меченого радиоактивным изотопом, выводится в течение 12 дней после его приема, при этом 71 % выводится через кишечник (47 % в виде исходного соединения и 24 % в виде метаболитов) и около 19 % - почками в виде глюкуронидов. В равновесном состоянии выведение глюкуронидов почками уменьшается и составляет меньше 10 %. Исходное соединение, обнаруженное в каловых массах, может быть продуктом желудочно-кишечного расщепления глюкуронидов, или продуктом восстановления метаболита М-2 (N-оксида), или остатком неабсорбированного препарата.
Линейность/нелинейность
Системное воздействие регорафениба при равновесной концентрации возрастает пропорционально дозе при дозе до 60 мг и менее пропорционально при дозах более 60 мг. Накопление препарата при равновесной концентрации приблизительно в два раза превышает концентрацию в плазме, которая соответствует периоду полувыведения и частоте приема лекарственного средства.
После перорального приема регорафениба в дозе 160 мг его средняя максимальная концентрация в плазме крови (Cmax) в равновесном состоянии достигает 3,9 мг/л (8,1 мкмоль). Соотношение максимальной и минимальной концентрации регорафениба в плазме крови составляет менее 2.
Для обоих метаболитов М-2 и М-5 свойственно нелинейное накопление в плазме крови. После однократного приема регорафениба концентрации метаболитов М-2 и М-5 намного ниже, чем у исходного соединения. В равновесном состоянии концентрации М-2 и М-5 сопоставимы с концентрацией регорафениба.
Фармакокинетика у различных групп пациентов
Пациенты с нарушением функции печени
У пациентов с легкой (класс А по классификации Чайлд-Пью) или умеренной (класс В по классификации Чайлд-Пью) степенью печеночной недостаточности, фармакокинетические параметры регорафениба были такими же, как у пациентов с нормальной печеночной функцией. У пациентов с тяжелой степенью печеночной недостаточности (класс С по классификации Чайлд-Пью) фармакокинетика регорафениба не изучена. Поскольку печень имеет большое значение в выведении регорафениба, у пациентов с тяжелым нарушением функции печени возможно усиление действия препарата (см. раздел «Особые указания»).
Пациенты с нарушением функции почек
У пациентов с легкой и средней степенью почечной недостаточности экспозиция регорафениба и его метаболитов М-2 и М-5 в равновесном состоянии является такой же, как у пациентов с нормальной функцией почек. У пациентов с тяжелой степенью почечной недостаточности или терминальной степенью почечной недостаточности фармакокинетика регорафениба не изучена.
Пациенты пожилого возраста
Влияние возраста на фармакокинетику регорафениба у пациентов от 29 до 85 лет не обнаружено.
Пол
Не выявлено различий в фармакокинетике регорафениба в зависимости от пола.
Этническая принадлежность
Не выявлено различий в фармакокинетических параметрах регорафениба в зависимости от принадлежности к этнической группе.
Электрофизиология сердца/удлинение QТ
У пациентов с онкологическими заболеваниями не было выявлено удлинение интервала QТ в равновесном состоянии при приеме регорафениба в дозе 160 мг.
Показания к применению
- Метастатический колоректальный рак у пациентов, которым уже проводилась или не показана химиотерапия фторпиримидиновыми препаратами, терапия, направленная против сосудистого эндотелиального фактора роста (VEGF) и терапия, направленная против рецепторов эпидермального фактора роста (EGFR);
- Неоперабельные или метастатические гастроинтестинальные стромальные опухоли упациентов при прогрессировании на терапии иматинибом и сунитинибом или при непереносимости данного вида лечения.
Противопоказания
- Повышенная чувствительность к регорафенибу или любому другому компоненту, входящему в состав препарата.
- Детский возраст до 18 лет
- Беременность и период грудного вскармливания (см. раздел «Применение при беременности и в период грудного вскармливания)
- Тяжелая степень печеночной недостаточности (класс С по классификации Чайлд-Пью).
- Тяжелая степень почечной недостаточности (опыт клинического применения отсутствует).
С осторожностью
Необходимо соблюдать дополнительную осторожность при назначении препарата в следующих ситуациях:
- при нарушениях функции печени легкой и средней степени тяжести;
- при наличии факторов риска кровотечения, а также при совместном применении с антикоагулянтами и другими препаратами, повышающими риск кровотечений;
- при ишемической болезни сердца.
Применение при беременности и в период грудного вскармливания
Фертильность
Не проводилось специальных исследований применения регорафениба для оценки его влияния на фертильность человека.
В исследованиях на животных наблюдалось снижение мужской и женской фертильности. Женщин репродуктивного возраста необходимо проинформировать об опасности препарата Стиварга® для плода. Во время лечения и в течение 8 недель после терапии препаратом Стиварга® женщины и мужчины репродуктивного возраста должны применять надежные методы контрацепции.
Беременность
Данные о применении препарата Стиварга® у беременных женщин отсутствуют.
Учитывая механизм действия регорафениба, возможно негативное влияние препарата Стиварга® на плод. Исследования на животных продемонстрировали репродуктивную токсичность регорафениба.
Период грудного вскармливания
Не установлено, выделяются ли регорафениб и его метаболиты с женским молоком.
Исследования на животных показали, что регорафениб и его метаболиты выделяются с грудным молоком.
Поскольку нельзя исключить возможность негативного влияния регорафениба на рост и развитие детей раннего возраста, следует прекратить грудное вскармливание в период лечения препаратом Стиварга®.
Способ применения и дозы
Для приема внутрь.
Препарат Стиварга® должен назначаться только врачом, имеющим опыт противоопухолевой терапии.
Рекомендуемая суточная доза препарата Стиварга® составляет 160 мг (4 таблетки по 40 мг). Препарат назначается один раз в сутки в течение 3 недель. В последующую неделю (4-я неделя от начала лечения) следует перерыв в приеме препарата. Период продолжительностью 4 недели от начала приема является одним курсом лечения препаратом Стиварга®.
Таблетки принимают каждый день (один раз в сутки) в одно и то же время после приема пищи, содержащей низкое (< 30 %) количество жира (см. раздел «Фармакокинетика»). Таблетки следует проглатывать целиком, запивая водой.
Если очередной прием препарата пропущен, пациент должен принять таблетку в тот же день, как только об этом вспомнит. Не следует принимать двойную дозу препарата в течение одного дня с целью компенсировать пропущенный прием.
В случае рвоты после приема препарата Стиварга® дополнительную таблетку принимать не следует.
Лечение продолжают до тех пор, пока сохраняется клиническая эффективность препарата или до появления его неприемлемого токсического действия (см. раздел «Особые указания»).
Коррекция дозы
Индивидуальная переносимость и безопасность лечения может потребовать временного прекращения терапии и/или уменьшения дозы препарата Стиварга®.
Коррекция дозы на каждом этапе снижения дозы составляет 40 мг (1 таблетка). Наименьшая рекомендуемая доза препарата Стиварга® составляет 80 мг в сутки. Максимальная суточная доза 160 мг.
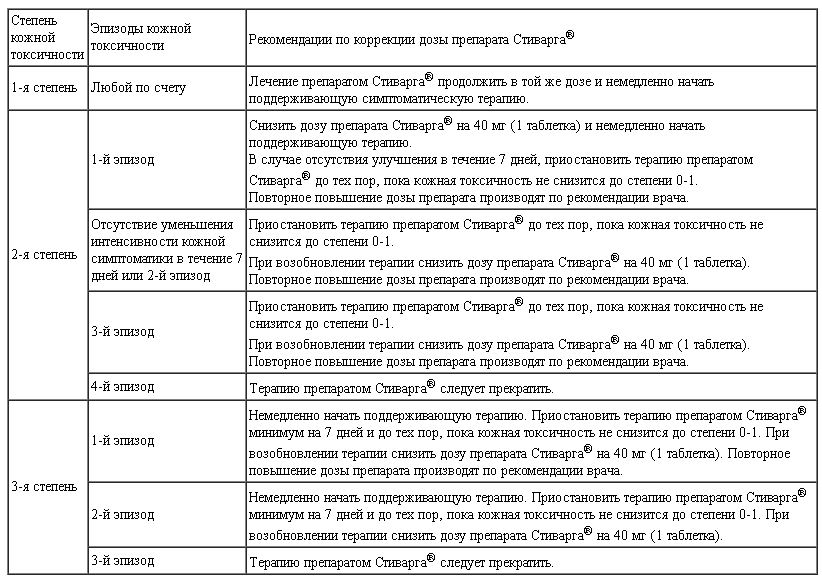
Таблица 1.
Рекомендации по коррекции дозы препарата Стиварга® при развитии ладонно-подошвенной эритродизестезии
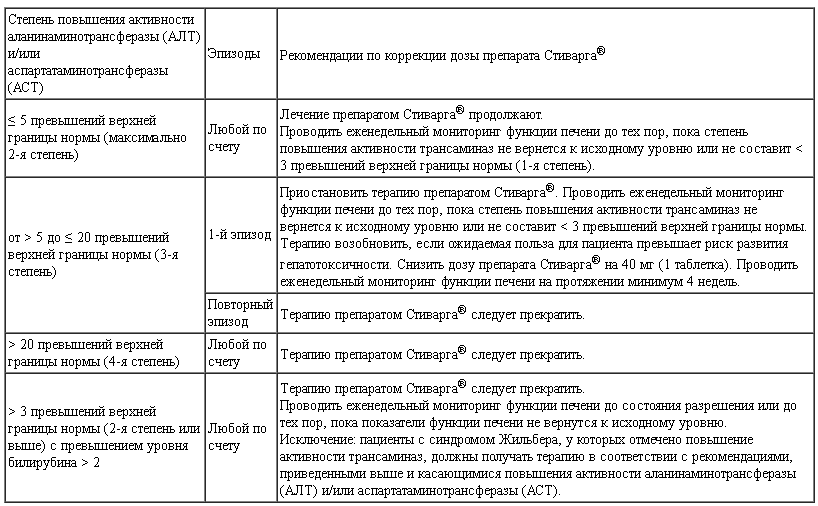
Таблица 2.
Рекомендации по коррекции дозы препарата Стиварга® при ухудшении биохимических показателей функции печени (см. раздел «Особые указания»)
Особые группы пациентов
Пациенты с нарушением функции печени
Печень имеет большое значение в выведении регорафениба. Не было выявлено клинически значимых различий в воздействии препарата Стиварга® у пациентов со средним (класс А по классификации Чайлд-Пью) и умеренным (класс В по классификации Чайлд-Пью) нарушением функции печени в сравнении с пациентами с нормальной функцией печени. Пациентам со средним и умеренным нарушением функции печени коррекция дозы не требуется. Рекомендуется проводить мониторинг функции печени на фоне терапии препаратом Стиварга® у данной категории пациентов (см. разделы «Фармакокинетика», «Особые указания»). Не рекомендуется лечение препаратом Стиварга® пациентов с тяжелым нарушением функции печени (класс С по классификации Чайлд-Пью), поскольку применение препарата у данной категории пациентов не изучено.
Пациенты с нарушением функции почек
В клинических исследованиях не отмечалось значимых различий безопасности и эффективности препарата Стиварга® у пациентов с легкой степенью почечной недостаточности (рСКФ 60-89 мл/мин/1,73 м2) в сравнении с пациентами с нормальной функцией почек. Ограниченные данные по фармакокинетике не выявили различий в экспозиции у пациентов со средней степенью почечной недостаточности (рСКФ 30-59 мл/мин/1,73 м2). Пациентам с легкой и средней степенью почечной недостаточности снижение дозы препарата не требуется (см. раздел «Фармакокинетика»). Применение препарата Стиварга® у пациентов с тяжелой степенью почечной недостаточности (рСКФ < 30 мл/мин/1,73 м2) не изучено.
Дети
Безопасность и эффективность назначения препарата Стиварга® у детей и подростков до 18 лет не установлена.
Пациенты пожилого возраста
В клинических исследованиях не отмечалось значимых различий безопасности и эффективности препарата Стиварга® у пожилых (65 лет и старше) пациентов в сравнении с более молодыми пациентами. Пациентам пожилого возраста коррекция дозы не требуется (см. раздел «Фармакокинетика»).
Пол
В клинических исследованиях не отмечалось значимых различий безопасности и эффективности препарата Стиварга® между пациентами мужского и женского пола. Коррекция дозы препарата в зависимости от пола пациента не требуется (см. раздел «Фармакокинетика»).
Этническая принадлежность
В клинических исследованиях не отмечалось значимых различий безопасности и эффективности препарата Стиварга® у пациентов разных этнических групп. Корректировка дозы препарата в зависимости от этнической принадлежности пациента не требуется (см. раздел «Фармакокинетика»).
Побочное действие
Общий профиль безопасности препарата Стиварга® оценивается на данных клинических исследований с участием более 1200 пациентов, получавших терапию в плацебо-контролируемых клинических исследованиях III фазы. Данная группа включала 500 пациентов с метастатическим колоректальным раком и 132 пациента с гастроинтестинальными стромальными опухолями.
Данный профиль безопасности регорафениба был подтвержден и в клиническом исследовании III В фазы с участием 2872 пациентов с метастатическим колоректальным раком при прогрессировании на стандартной терапии.
В клинических исследованиях наиболее частыми нежелательными реакциями (≥ 30% пациентов) были астения/усталость, ладонно-подошвенная эритродизестезия, диарея, снижение аппетита и потребления пищи, повышение артериального давления, дисфония, инфекции.
Наиболее серьезными нежелательными реакциями при приеме препарата Стиварга® были поражения печени, кровотечения, прободение желудочно-кишечного тракта.
Перечисленные ниже нежелательные явления, отмеченные при применении препарата Стиварга® в ходе клинических исследований, распределены по частоте возникновения в соответствии со следующей градацией: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥ 1/1000 до <1/100), редко (от ≥ 1/10000 до <1/1000). Для классификации и описания конкретной реакции, ее синонимов и связанных с ней состояний, используется наиболее подходящий термин из Медицинского словаря для регуляторной деятельности (MedDRA).
В каждой частотной группе нежелательные явления представлены в порядке уменьшения их значимости.
Нарушения со стороны крови и лимфатической системы
Очень часто: тромбоцитопения, анемия.
Часто: лейкопения.
Нарушения со стороны сердца и сосудов
Очень часто: кровотечения*, повышение артериального давления.
Нечасто: инфаркт миокарда, ишемия миокарда, гипертонический криз.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Очень часто: дисфония.
Нарушения со стороны кожи и подкожных тканей
Очень часто: ладонно-подошвенная эритродизесте
Обратная Связь
Новости
Открытие: ДЦП передается от родственников
Считается, наследственность не является
подробнее...Привычка грызть ногти приводит к инфекциям
Грызть ногти вредно
подробнее...Первый кардиостимулятор
Генетики получили первый биологический кардиостимулятор
подробнее...Эпидемия Эбола принимает плохой оборот
Месяц назад весь мир узнал о том, что в Африке
подробнее...